ユーザーズボイス
CELL HANDLER™をご活用いただいているお客様の声をご紹介します。
「CELL HANDLERがなければ、成立しなかった」
——3D培養環境下のクローン分離を可能にした自動化
培養器の中で病態を再現し、疾患の仕組みを細胞レベルで理解する。近年はゲノム編集技術を用いて特定の遺伝子変異を持つ細胞を作製し、疾患モデルとして解析する研究が進んでいます。その過程では、目的どおりの遺伝子改変がおこなわれた細胞クローンを単離し、次の評価へつなげる工程が重要になります。
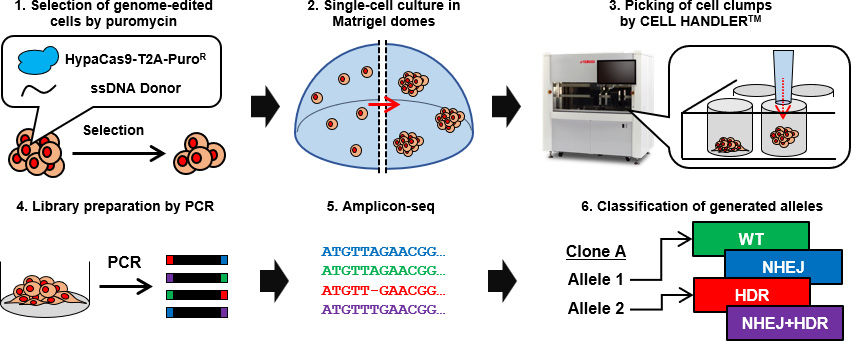
一般的なクローン単離では平面培養での操作が多い一方、今回の研究ではiPS細胞を3D培養環境で維持しながらクローンを扱う新しいアプローチを検討しました。ゲル内で形成されるクローンの中から目的のものを正確に回収できるかどうかが、この実験の成功を大きく左右します。
公益財団法人 東京都医学総合研究所 再生医療プロジェクト 宮岡研究室では、ヒトiPS細胞とゲノム編集技術を用いて、患者さんの遺伝情報を手がかりに病態を再現し、疾患の原因やメカニズムを実験的に確かめる研究に取り組んでいます。今回のインタビューでは、研究の狙い、iPS細胞研究における実験上の課題、そしてCELL HANDLER™を使用したことで見えてきた価値について、宮岡佑一郎氏に伺いました。

東京都医学総合研究所
再生医療プロジェクト
プロジェクトリーダー
宮岡佑一郎氏
細胞で病気を理解し、治療の可能性を広げる
Q. 現在の研究テーマに至った経緯を教えてください。 博士課程修了後にサンフランシスコへ留学し、研究室を移ることになったとき、たまたまiPS細胞とゲノム編集を扱う研究室に入ったことが転機になりました。出会いとしては偶然だった部分もありますが、実際に取り組む中で、病気の理解や治療につながる研究の面白さを強く感じました。細胞の段階で病気の成り立ちを捉え、その原因に迫ることが将来的に根本的な治療につながり得る、その可能性に惹かれて今の研究につながっています。
Q. 宮岡研究室として、どのような価値を社会に届けたいと考えていますか。
患者さんの遺伝子疾患を細胞モデルを用いて再現し、発症メカニズムの理解につなげたいと考えています。病気の細胞の状態を研究室で再現できれば、なぜその病気が起きるのかを調べることができるだけでなく、薬を加えて改善するかどうかを検証することも可能になります。まずは基礎研究として疾患の本質を理解することが重要です。
病気のメカニズムを知れば知るほど、治療のアプローチは増えていきます。だからこそ、「知ること」を丁寧に積み重ねることに価値があると感じています。
その積み重ねが将来的に創薬や、さらには細胞を患者さんに戻すような治療につながる可能性もあります。研究の成果が最終的に患者さんの役に立つかたちになればと考えています。
Q. 研究テーマを決めるときに大切にしていることはありますか。
方向性としてはできるだけ患者さんの治療にどう役立つかがイメージできること、そして新規性があることの両方を意識しています。一方で、夢だけ語っても実現できないと意味がないので、実現可能性とのバランスも取る必要があります。
ある研究では、家族内で同じ心房中隔欠損がありつつ、一部の方だけ別の心機能の病態が出るケースがありました。患者さんから出た遺伝子情報をiPS細胞とゲノム編集技術を用いて再現し積み重ねることで、「相関」だけではなく「因果」に近づいていく、そういう研究の進め方を大事にしています。
Q. iPS細胞×ゲノム編集の研究で、いま大きなボトルネックだと感じている点は何でしょうか。
私たちの研究では心疾患に加えて、肝疾患や神経疾患も扱っています。対象が変わっても「遺伝子情報がどう表現型につながるかを実験で確かめる」という軸は共通です。
また、臨床現場では疾患の遺伝子変異情報が蓄積していく一方で、細胞実験で確かめる側の負荷が大きい現状があります。そのため、iPS細胞での病態再現検証を効率的に回せる基盤づくりも重要だと感じています。
CELL HANDLER™への期待—— iPS細胞での病態再現を効率化できる基盤
Q. CELL HANDLER™を使うきっかけと、研究の中での役割を教えてください。
きっかけはとある企業様からの紹介でした。先にセルソーターを扱う企業と共同研究をしていて、「ヤマハ発動機さんの良い機械がある」と教えてもらったのが最初です。セルソーターのアプローチではiPS細胞を単離すると細胞死が誘導され、実験に適さない部分がありました。
そこで3D培養環境下でiPS細胞のクローンを「見て・選んで・取る」工程にCELL HANDLER™が適していました。
研究の中では、iPS細胞のゲノム編集後にクローンを単離する工程で使用しました。実際のiPS細胞集団を確認しながら欲しいクローンをコンタミなく単離できたことに驚きました。
Q. 2D平面培養のコロニー操作と比べたとき、3D培養の利点・欠点はありますか。
多くのクローンが必要なときは、3Dで扱うと一つのウェルから取れるクローン数が増やせるという感覚があります。2Dにしたときより数が稼げるので、スループットの面でメリットが出やすいです。一方で手間がかかるのも事実です。ただ、数が増えてくれば必要な培地量を減らせる可能性もあり、条件によってはコスト面でもメリットがあると思います。
最大の障壁は「CELL HANDLER™が使える環境があるかどうか」だと感じます。逆に言えば、使える環境があるなら、3Dでクローン数を稼ぎつつ評価につなげられるので、従来法より優位性が出せると思います。
3Dでの難しさとしては2Dと違って、クローンの位置や状態が一様ではないことです。狙った対象を見つけて、必要なものだけを回収して、次の工程につなぐ、この一連の流れを安定して行うこと自体が難しくなります。
Q. 実際に使ってみて驚いた点・良かった点はどこですか。
3D培養環境下で分取する必要があるので難易度が高いのでは、と最初は思っていましたが、サンプル分取は初期からうまくいきました。XY方向だけでなくZ方向も制御しクローンを狙えたのは、さすがだと思いました。
精度が良く、ピッキング後のクローンへのダメージも「ほとんどないのでは」という感触でした。もちろん条件出しは必要ですが、クローンの位置を認識し画像としても適切なクローンか判別して、そこに正確に取りに行く、この精度は他で代わりがない。CELL HANDLER™がなければ、成立しなかったというのが率直な印象です。
それと、装置そのもの以上に印象に残っているのは、ヤマハ発動機スタッフの方々の姿勢です。「この機械ではここまでしかできない」と最初から線を引くのではなく、「まず試してみましょう」というチャレンジ精神と開発魂が強く記憶に残っています。初期の検討で条件や可能性を具体化できたのは助かりました。
Q. 「CELL HANDLER™がなければ、成立しなかった」と感じた理由を教えてください。 今回の研究では、iPS細胞を3Dのゲル培地中で培養した状態から、目的のクローンを選んで回収する必要がありました。3D培養環境下のクローンを人の手で狙って回収するのは、現実的ではありません。この実験はCELL HANDLER™がなければ、成立しなかったと確信しています。
今後の展望——因果を確かめる実験をより早く・より確実に回すために
Q. 今後の研究の展望について教えてください。
臨床現場では「この患者さんはDNAのこの部分がおかしい」といった遺伝子変異情報がどんどん蓄積しています。一方で、遺伝子変異と病態の相関だけが分かっていて直接の原因であるかどうかは分からないことが多いです。因果関係を調べるには実験的に細胞モデルを作るしかありませんが、一つひとつ試すのは大変なので、そこをもっと効率化できないかと検討しています。
ゲノム編集iPS細胞を効率的に樹立し、遺伝子情報が表現型に与える影響を試せるシステムを作っていきたい。その先で病気と遺伝子情報の因果を明らかにし、治療戦略の多様化、創薬の効率化にも寄与できればと考えています。
臨床で見つかった遺伝子変異候補を、実験で素早く評価できるようになれば、どこが本当に治療標的になり得るのかをより確かなかたちで示せます。そのための“試せる基盤”を整えることが、今後ますます重要になると考えています。
Q. CELL HANDLER™に期待することはありますか。
CELL HANDLER™の特徴は、顕微鏡観察と細胞分取を同一の装置内で行える点にあると思います。
従来のセルソーターは高いスループットを持つ一方で、細胞の挙動や時間的な変化といった情報を確認しながら選別することは難しい場合があります。CELL HANDLER™では、細胞の状態を一定時間観察しながら選択できるため、これまでとは異なる視点でのセルソーティングが可能になるのではないかと感じています。
例えば、連続画像撮影などで、動的な挙動や経時的な変化指標を満たす細胞を自動で見つけ出し、そのまま分取までつなげられるようになれば、新たな評価手法の確立につながります。
このようにCELL HANDLER™でしか選別できない細胞特徴パラメータが拡張され、研究現場で広く使われる基盤になっていくことを期待しています。